�������: 1-15 ���鵽����ѧ ���Գƺϳ�����ؼ�¼55�� . ��ѯʱ��(0.1 ��)

�Ϻ��Ƽ���ѧ���ʿ�ѧ�뼼��ѧԺ�ߵ�ΰ������ʵ��1,3-�������ĵ�˫�����������Գƺϳ���ͼ��
1,3-�������� ˫������ ���Գƺϳ�
2024/3/4

�й��ƴ��������ɻ������Գƺϳ�����ȡ�ý�չ��ͼ��
�� �ϳ� ���� ���ӻ�ѧ
2023/12/1
�й���ѧ������ѧ�����ܻ�ѧ�ص�ʵ���ҽ�������ᡢ��Ң�������ŷ��������о��Ŷӣ���չ��һ�����������ɻ��������Գ����칹����Ӧ���ù�����ƿ�����һ��ṹ����ȫ�µ����Ե��ӿ���-�����ɻ�����������չ�������ɻ��������Գ������칹����Ӧ��2023��12��1�գ�����о��ɹ����߷����ڡ���ѧ����Science��DOI��10.1126/science.adg1322���ϡ�
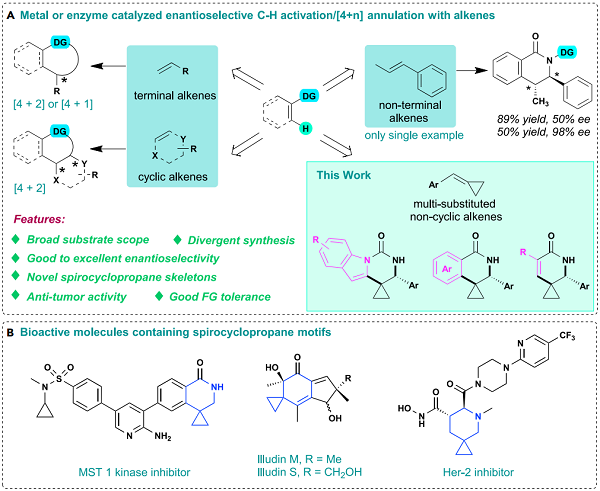
�����ݻ�һ����Ҫ��ҩ�����ƹǼܣ��㷺��������Ȼ�����ҩ������У�������Ҫ������ѧ���ԣ�����θ�Ч������Щ�ṹ���ӵ��ݻ��Ǽ��Ծ���ս��Ҳ���л��ϳ������о����ѵ���ȵ�֮һ���ڹ�ȥ�ļ�ʮ������ɽ����������Գ�C-H�����Ϊ�ǹ������ԹǼܵ�һ�ָ�Ч�����ķ������ڱ����ķ�Ӧ��ͨ������ĩ��ϩ���ͻ�ϩ����Ϊ��Ҫ���ϳ������������ӵĶ�Ǽܣ�����ȡ���ķǶ�ϩ�������ڿռ�λ��ͷ�Ӧ���Եͣ������Գ�C-H��...
�й���ѧԺ������ѧ�����о���ר����һ���ɦ�-ͪ�����Գƺϳ����Ԧ�-��Ȳ��ͪ�ķ���
�й���ѧԺ������ѧ�����о��� ר�� ��-ͪ�� ���Գƺϳ� ���Ԧ�-��Ȳ��ͪ
2023/9/6

�й���ѧԺ�Ϻ�ҩ���о��������Ŷӳ���������̼��������Ч�ϳ�����ѧ�����ഴ��ҩ���о���2020�귢չ��C(sp3)-H����ٹ������̼�������ĸ�Ч�ϳ�������ʵ���˰������ λ̼���������ϳ�(Angew.Chem.Int. Ed. 2020, 59,3491�C3494) ��2021������Ը�Ч̼�����Է�չ�˦� ���ͷ���̼�������ĸ�Ч�ϳ�������ʵ��������-C2-������̼�յ�����ѡ��...

���������ǰ����м��Եĵ�ԭ�Ӻ��ڼ����ܼ������õ��ܽ��ԣ���һ�����DZ��Ӧ�ü�ֵ��������ӵ����壨ͼ1����Ŀǰ���ϳ�����������Ҫ�����ǻ������Ե��������רһ��ת�����������������ǰ��������������ǰ��������������ǻ�������S�����Ż��������������ù��ɽ����������Գ�C-H�����ʽ��Ϊ�ϳ����������ǰ��ṩ����˼·��Ȼ�������ֹ��������˻�״�����ǰ������ڷǻ�״�����ǰ�����Ҫ�ԣ��������Գ�C-H����...

���գ�����������ѧҩѧԺ�ڴ����Գƺϳ�����ȡ���½�չ����سɹ��ԡ��ֺ�ҿЭͬ��ԭλ���ɶ�ϩ���Ħ�λ���Գ�ϩ����ȡ����Ӧ��Ϊ�ⷢ���ڡ��¹�Ӧ�û�ѧ����

���գ�����������ѧ����ƽ���ں������ָ������Ŷ�������Ԫ�ӻ��Ǽܴ����Գ������о���ȡ�����½�չ������о��ɹ��ԡ������Գ�ϩ����ȡ��/����������Ӧ��������Ԫ�ӻ��Ǽܡ�Ϊ�ⷢ����������ѧ�����־��

���¹�Ӧ�û�ѧ����������������ѧ�ڴ����Գƺϳ����������о���չ��ͼ��
����������ѧ �� ���Գƺϳ� �����Գ�
2019/12/6
���գ���УҩѧԺ�Ϻ�����ҩ����ص�ʵ���ҵ���ƽ�����Ŷӣ��ڽ����ٴ����Գ�[4+3]���ӳɷ�Ӧ��Ч�ϳ����Ե����������о���ȡ������Ҫ��չ������о��ɹ������ڡ��¹�Ӧ�û�ѧ���ϡ����������ƹǼܹ㷺�����ڶ���ҩ����Ӻ���Ȼ���Ի������У����Ч����һֱ���л��ϳ��ʹ���ҩ���о�������Ҫ���о��ȵ�֮һ��[4+3]���ӳɷ�Ӧ��Ϊ������Ԫ���Ǽ���ֱ�ӡ���Ч���ֶ�֮һ�����ִ��л��ϳ����������ҪӦ�á�Ȼ��...

���Ŵ�ѧ��ѧ����ѧԺ���ڿ�����ɼ�������ͭ�����Գƺϳ���չ������nature communications��ͼ��
���Ŵ�ѧ��ѧ����ѧԺ ���� �ɼ�������ͭ �����Գ�
2019/9/5
��ѧ����ѧԺ���ڿ������ڿɼ�����������ͭ���ǻ��ǰ������Գ���-����������о���ȡ�ý�չ����ؽ����Photocatalytic enantioselective ��-aminoalkylation of acyclic imine derivatives by a chiral copper catalyst���ڽ��շ����ڡ���Ȼ•ͨѶ����Nat. Commun. 2019, 10, ...

�й���ѧԺ�Ϻ��л���ѧ�о����ڴ����Գƺϳ�������̼�����о���ȡ�ý�չ��ͼ��
�й���ѧԺ�Ϻ��л���ѧ�о��� �����Գ� ������̼����
2018/4/19
�й���ѧԺ�Ϻ��л���ѧ�о������ۻ�ѧ�ϳ�����ʵ����л��ΰ������һֱ�����ڷ�չ���ɽ�����ѡ����̼����BHλ������Ż���������ǰ�ڷ�չ���ٴ�������B−H�����������������ϣ�J. Am. Chem. Soc. 2015, 137, 3502����ͨ�����Բ�ּ�������ȷ����һ����-̼���������4/5-λB−H��ѡ���Է���������ľ������幹�͡����������Ե������(R)-BI-DIM...
�ʻ���ԭøCR2����ø��ϵ���Գƺϳ�(S)-N,N-����-3-�ǻ�-3-(2-���)-1-����
����� ø ����ø��ϵ ���Գƻ�ԭ (S)-N,N-����-3-�ǻ�-3-(2-���)-1-����
2019/1/21
�������ʻ���ԭøCR2����ø��ϵ�����Ż�����ص�ø�ٴ���Ӧ����.ͨ���ڴ���ϵ�����Ӹ�øNADP+��0.1 mmol/L�������������ǣ�120 g/L������30�漰pH=8.0�������·�Ӧ4 h��CR2����ø��ϵ���Գ���ԭN��N-����-3-ͪ-3-��2-��ԣ�-1-������DKTP��10 g/L�����ϳ��˸߹�ѧ���ȣ�S��-N��N-����-3-�ǻ�-3-��2-��ԣ�-1-����[��S��-DHTP��...
����ʦ����ѧ�ϳ���ѧ�μ��ھ��� ���Գƺϳ���

�й���ѧԺ�Ϻ��л���ѧ�о������л�����������Գƺϳ�����ȡ�ý�չ��ͼ��
�й���ѧԺ�Ϻ��л���ѧ�о��� �л������� ���Գƺϳ�
2016/5/13
��״���������ִ��л���ѧ��ռ������Ҫ�ĵ�λ����״�ṹ�㷺�����ڸ�����Ȼ����;�����Ҫ�������Եķ����У���ˣ��������������ϳ��Ǽ�����Ҫ�ġ���ĿǰΪֹ����ѧ�����Ѿ���չ�˴����ķ����ϳ�С�������������Ԫ��)������Diels�CAlder��Ӧ���������ӳɷ�Ӧ�ȡ����ڴ�����RʮԪ����ͬ��Ҳ�кܶ��ϳ�����������Corey�CNicolaou����������Ӧ��Keck����������Ӧ��ϩ�����ֽⷴӦ�ȡ�...

2015��3��18�գ��й���ѧԺԺʿ�������������콲̳��93���߳���ѧ����̳��7�ڣ�������Ϊ�����������Գƺϳ���ʮ�꡷�Ľ����������˹�������������Գ��ķ�չ��ʷ�����������Ƚ����˴��Գ��Ļ�ѧ�������Գ��Ļ�ѧ���ķ�չ���̣��Լ������������Ҫ�ԣ����Ŵ���������е��Գ��ԡ������еĹǼ����ԡ���λԭ�ӵķ�չ�������о��ƶ����µķ�չ��������չ��������
�й��о����������а�-��
- ���ڼ���...
�й�ѧ���ڿ����а�-��
- ���ڼ���...
�����ѧ���л������а�-��
- ���ڼ���...
�й���ѧ���а�-��
- ���ڼ���...
�ˡ���-ƪ
- ���ڼ���...
�Ρ���-ƪ
- ���ڼ���...
��������-ƪ
- ���ڼ���...
�������� -ƪ
- ���ڼ���...
֪ʶҪ��-ƪ
- ���ڼ���...
���ʶ�̬-ƪ
- ���ڼ���...
��������-ƪ
- ���ڼ���...
ѧ��ָ��-ƪ
- ���ڼ���...
ѧ��վ��-ƪ
- ���ڼ���...


